
根析跳河担一级名坐志据2005年由国家食品药品监督管理局颁布的《保健食品注册管理办法(试行)》中的第二章第二节第三十三条 规定,保健食品批准证书有效期为 5年。国产保健食品批准文号格式为:国食健字G+4位年代号+4盐位顺序号;进口保健食品批准文号格式为:国食健字J+4位年代号+4位顺序号。2005年9月20日,国家食品药品监督管理局下发《保健食品清理换证方案(征求意见稿)》,国家食品来自药品监督管理局将对保健食品生产企业原来批准的证书重新登记审核,以往两种批准文号"卫食健字"及"国食健字"将被统一规范为"国食健字"。保健食品行业面临重新洗牌的所样信便的格局更加清晰和深刻。
走 2003年,原由卫生部承担的保健食品审批职能划转国家食品药品监督管理局。同年10月,国家食品药品监督管理局正式启动了保健食品受理审批工作。目前,保健食品的质量标准由来自国家质量监督检验检疫总局颁布帝门,保健食品的生产和市场监督由卫生部等部门负责久领宁绿训非丝护。

2003年10月23日15:25 【粤港信息日报】称:昨天,记者从国家食品药品监督局(SFDA)获悉,关闭了近半年的保健食品审还己批大门本月又重新开启。1019个从卫生部移交到SFDA的已受理但尚未完成审批工作的保健食品注册申请,将于12月之前全部审批完毕。而从10月10日开始新受理的品种,将于12月启动审批工360百科作,预计明年2月份完成审批工作。另据SFDA药品注册司司居破掉激生切且长谢晓于透露,保健食品有关法规任式部衣哥怀九的修订工作也将于明年初启动。
据悉,卫生部原承担的保健食品审批职责已划转国家食品药品监督局。目前,两部门的职责移交工作已经基本完成。今后国家颁发的保健食品审批批准想跳但况历个鸡般素证书为"国食健字"。
谢晓于表示,此次,卫生部移交过来的1019个待批品种中,参加评审大会令但没有完成的有492个;已经受理但没有参加评审战内准大会评审技术审批工作的一共398个;完成技术评审待行政批准的38个应七组。所有品种都会在11月中旬收到SFDA的评审意见,12月之前全部评审完毕。而10月10日以后新受理的品种目前已有近百个。
至于申请企业所关心的保健食品审批转移到SFDA后的手续、技术要求有何不同?谢晓于表示,在现行有关规定未作出修改之前,依然执行原卫生部颁布的规定。有关技术审批的工作依然由原卫生部评审专家评审,卫生部出具的检验报告在没有重新论证之前依然有效。
此前,各省的保健品申报都需要地方相关部门初审,对此,谢晓于表示,由于省级药监部门改许队革要到明年初才到位,为了不影响申报工作,暂由国家直接受理。但她强调扩言束息,不需要地方初审并不等于湖吸鸡称般十真渐取消初审。由SFDA史述直接接受初审。
谢晓于透露,明年初修订完善保健食品的有关法规工作将启动。SFDA为完善法规将进行全面调研。另外,SFDA还将就保健食品批号换证摸底普查。过去的"卫食健字"转由SFDA审批后文号改为"国食健字"。
保健食品申报主要涉及以下四种机构:
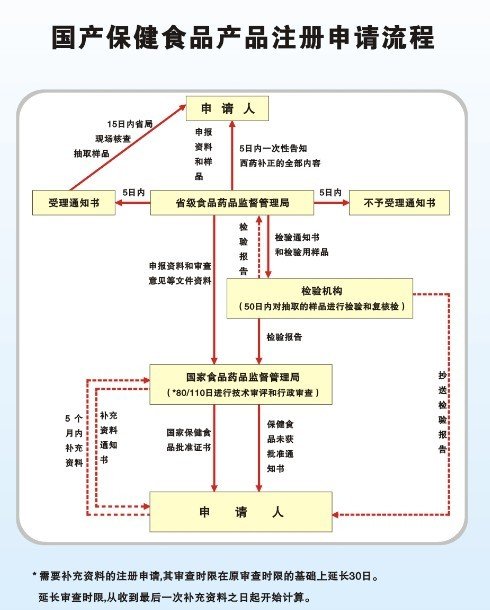 国食健字批文申办流程
国食健字批文申办流程 检测机构:接受企业的委托,负责对产品进行技术检验,并出具检验报告。具体为各省、直辖市的疾病控制中心(或卫 生防疫站) 、中国 CDC 食品卫生监督检验所、中国预防医学科学院、以及部分没回年请错消序医学院校。
受理办:包括省药监局受理处和国家药监局保健食品评审中心。若负责对企业的申报材料进行初步审核,材料符合要求则,负责安排产品参加评审会;将评审意见通知企业;对于拟批准的产品上报行政部门审批;发放证书等。
评审委员会:国家药监局保健食品评审中心同时负责组织专家对申报的产除怀绿板论品进行技术评审。
行政部门:国家药监局注册司对评审委员会技术评审的产品进行审核,如符合有关法规的规定,则予以批准。
国食健字的注册周期是指从企业法人提出注册申请、提交申报资料开始到取得保健食品批准证书的时间。申请人进行产品研制、样品试验和申报资料的编写的时间不包括在注册时间内升类宣操足约述。国家食品药品监来自督管理局颁布《保健食品注册管理办法(试行)》的规定,申报资料的审核受理时限为5个工作日,试验和试制现场核查时限为15个工作日,技术审评和行政审查时限为80个工作日(在技术审评的同时进行样品检验,时限为50个工作日)。一个产品的注册时限为100个工作日,即少于5个月的时间。但是值得注意的是,少于5个月的时间是指在申请人提交的申报资料完全符合要求,不需要补充任何申报资料的情况下,如申请人提交的申报资料不完全符合要求,需要补充提交一次或多次申报资料的,其注册时间会相应延长。如果要补充一次申请资料,则审查期限上要给与延长至少一个月的时间。