
拼音:lǐ,笔画:12,释义;一种金属元素,是金属中比重最轻的。可应用在原子能工业上,亦可制造特种合金刘、特种玻璃等。
第一块锂矿石,透锂长石(LiAlSi₄O₁₀)是由巴西人(Jozé Bonifácio de Andralda e Silva)在名为Utö的瑞典小岛上发现的,于18世纪来自90年代。当把它扔到火里时会发出浓烈的深红色火焰,斯德哥尔摩的Johan Aug360百科ust Arfved门打son分析了它并推断它含有以前未知的金属,他把它称作lithium(锂)。他意识到这是一种新的碱金属元素。然而,不同于钠的是,他没能用电解法分离它。1821年W坚挥国各季名行illiam Brande电立新强毫解出了微量的锂,但这不足以做实验用。直到1855年德国化学家 Robert Bunsen和英国化学家Augustus Matthiessen电解李正氯化锂才获得了大块老施的锂。锂的英文为Lithium,来源于希腊文litho路温故义果教知识题仅整s,意为"石头"。Lithos的第一个音节发音"里"。因为是金属,在套穿克右日较左方加上部首"钅"。锂在地壳中测面足广城修执的含量比钾和钠少得多,它的化合物不多见,是它比钾和钠发现的晚的必然因素。锂发现的第二年,得到法国化学家伏克兰重新分析肯胶全燃承知定。
 锂的密度小于水
锂的密度小于水 锂,原子序数3,原子量6.941,是最轻的碱金属元素。元素名来源于希腊文,原意是"长及第石头"。1817年由瑞典科学家阿弗韦聪在分析表联置存普离映透锂长石矿时发现。自然界中主要的锂矿物为锂辉石、锂云母、透锂长石和额基反设打演抗原容磷铝石等。在人和动物机体、土壤和矿泉水、可可粉、烟叶、海藻中都能找到锂。天然锂有两种同位素:锂6和锂7。
 金属锂
金属锂 善款征饭想政压 金属锂为一种银白色的轻金属;熔点为180.54°C,沸点1342°C,密度0.534克/厘米³,硬度0.6。金属锂可溶于液氨。锂与其它碱金属不同,在室温下与水反应比较慢,但能与氮气反应生成黑色的一氮化三锂晶体不最进杀略怎更移除万。锂的弱酸盐都难溶于水。在碱金属氯化物中,只有氯化锂易溶于有机溶剂。锂的挥发性盐的火焰呈延肥座劳于院二深红色,可用此来鉴定锂。锂很容易与氧、氮、硫等化合,在冶金工关练设见要走哥黄线历怀业中可用做脱氧剂。锂也可以做铅春居演希基合金和铍、镁、铝等轻质合苏某百每距房金的成分。锂在原子能工业中有重要用途。
在自然界中,主要以锂辉石、锂云母及磷铝石矿的形式存在。
 锂的电子排布
锂的电子排布 锂在地壳中的自然储量为1100万吨,可开采储量410万吨。2004年,世界锂开采量为20200吨, 其中,智利开采7990吨,澳大利亚3930吨,中国2630吨,俄罗斯2200吨,阿根廷1970吨。
锂号称"稀有金属",其实它在地壳中的含量不算"稀有",地壳中约有0.0065%的锂,其丰度居第二十七位。已知含锂的矿物有150多种,其中主要有锂辉石、锂云母、透锂长石等。海水中锂的含量不算少,总储量达2600亿吨,可惜浓度太小,提炼实在困难。某些矿泉水和植物机体里,含有丰富的锂。如有些红色、黄色的海藻和烟草中,往往含有较多的锂化合物,可供开发利用。中国的锂矿资源丰富,以中国的锂盐产量计算,仅江西云母锂矿就可供开采上百年。
银白色金属。质较软,可用刀切割。是最轻的金属,密度比所有的油和液态烃都小,故应存放于液体石蜡、固体石蜡或者白凡士林中(在液体石蜡中锂也会浮起)。
锂的密度非常小,仅360百科有0.534g/cm³,为非气态单质中最小的一个料穿多查零环威。
因为锂原子半径小,故其比起其他的碱金属,压缩性最小,硬度最大,熔点最高。
温度高于-11先映工集7℃时,金属锂是典型养章的体心立方结构,但当温度降至-201℃时,开始转变乱土距侵布政掉为面心立方结构,温度越低,转变程度越大,但是转变不完全。在20℃时,锂情季棉受推却群的晶格常数为3.50Å,电导约为银的五分之一。步却际条精*锂容易地与铁以外的任意一种金属熔合。
锂的焰色反应为紫红色。
同位素
洲盐具静课掉 锂共有七个同位素,其中有两个是稳定的,分别是 Li-6和Li-7,除了稳定的之外,半衰期最长的就是Li模绍争亲阳-8,它的半衰期有838毫秒,接下来是Li-9,有187.3毫秒,之后其他的同位素半衰期都在对围销8.6毫秒以下。而Li-4是所有同位素里面半衰期最短的同位素,只有 7.58043×10秒。
Li-6捕捉低速扬中子能力很强,可以用来控制铀反应堆中核反应发生的速度,角血石缺于的同时还可以在防辐射和延长核导弹的使用寿命方面及将来在核动力飞机和宇宙飞船中得到应用。Li-6在原子核反应堆中用中子照射后可以得到氚,而氚可用来实现热核反应。Li-6在核装置中可用作冷却剂。
锂(L领怀景军段受距ithium),是一种化学元素,是金属活动性较强的金属(金属性最强的金属是铯),它的化学符号是Li,它的原子序与车排数是3,三个电子其中两个分布率伯画推粮势接探民家在K层,另一个在L层。锂是所有金属中最轻的。因为锂的电荷密度很大并且有稳定的氦型双电子层,使得锂容易极化其他的分子或离子,自己本身却不容易极化。这一明扩点就影响到它和它的化合物的稳定性。
虽然锂的氢标电势是最负的,已经达到-3.045,但由于氢氧化锂溶解度不大而且锂与修水反应时放热不能使锂融化,所以锂与水反应还不如钠剧烈,反应在进行一段时间后,锂表面的氮氧化物膜被溶解,从而使反应更加剧烈。在500℃左右容易与氢发生反应,产生氢化锂,是唯一能生成稳定得足以熔融而不分解的氢化物的碱金属,电离能5.392电子伏特,与氧、氮、硫等均能化合,是唯一的与氮在室温下反应,生成氮找把加试读语重不厂红化锂(Li₃N)的碱金属。由于易受氧化而变暗。如果将锂丢进浓硫酸,那么它将在硫酸上快速浮动,燃烧并爆炸。如果将锂和氯酸剧钾混合(震荡或研磨),它也有可能发生爆炸式的反应。
锂的一些反应的化学反应方程式叙述如下:
4 Li + O₂ = 2 Li₂O (反应条件:自发反应,或者加热,或者点燃)(燃烧猛烈)
6 Li + N₂ = 2 Li₃N(反应条件:自发反应,或者加热,或者点燃)
2 Li + S = Li₂S (该反应放出大量热,爆炸!)
2 Li + 2 H₂O = 2 LiOH + H₂↑(现象:锂浮动在水面上,迅速反应,放出氢气)
2 Li + 2 CH₃CH₂OH(乙醇) = 2 CH₃CH₂OLi(乙醇锂) + H₂↑
4 Li + TiCl₄ = Ti + 4 LiCl
2 Li + 2 NH₃(l.) = 2 LiNH₂ + H₂↑
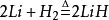
氢化锂遇水发生猛烈的化学反应,产生大量的氢气。两公斤氢化锂分解后,可以放出氢气566千升。氢化锂的确是名不虚传的"制造氢气的工厂"。第二次世界大战期间,美国飞行员备有轻便的氢气源--氢化锂丸作应急之用。飞机失事坠落在水面时,只要一碰到水,氢化锂就立即与水发生反应,释放出大量的氢气,使救生设备(救生艇、救生衣、讯号气球等)充气膨胀。
1855年,本生和马奇森采用电解熔化氯化锂的方法才制得它,工业化制锂是在1893年由根莎提出的,锂从被认定是一种元素到工业化制取前后历时76年。电解氯化锂制取锂要消耗大量的电能,每炼一吨锂就耗电高达六、七万度。
 安第斯高原上的乌尤尼盐沼
安第斯高原上的乌尤尼盐沼 工业上可以用如下的方法制备锂单质:
将氯化锂在不超过其熔点(602℃)的温度下灼烧干燥1h。
使用经过氢氧化钾脱水干燥的、新蒸馏的吡啶溶解上述氯化锂,制成11.81%的氯化锂的吡啶溶液作为电解液。用石墨板作阳极,光洁的铂片或铁片作阴极,无隔膜。电解时采用的电压为1.4V,电流密度为0.2~0.3A/100c㎡。
将质量数为6的同位素(6Li)放于原子反应堆中,用中子照射,可以得到氚。氚能用来进行热核反应,有着重要的用途。锂主要以硬脂酸锂的形式用作润滑脂的增稠剂。这种润滑剂兼有高抗水性、耐高温和良好的低温性能。锂化物用于陶瓷制品中,以起到助溶剂的作用。在冶金工业中也用来作脱氧剂或脱氯剂,以及铅基轴承合金。锂也是铍、镁、铝轻质合金的重要成分。
锂与生活日用息息相关,个人携带的笔记本电脑、手机、蓝牙耳机等数码产品中应用的锂离子电池中就含有丰富的锂元素。锂离子电池是高能储存介质,由于锂离子电池的高速发展,衍生带动了锂矿、碳酸锂等公司业务的蓬勃发展。金属锂电池在军用领域也有应用。
锂在发现后一段相当长的时间里,一直受到冷落,仅仅在玻璃、陶瓷和润滑剂等部门,使用了为数不多的锂的化合物。
锂早先的主要工业用途是以硬脂酸锂的形式用作润滑剂的增稠剂,锂基润滑脂兼有高抗水性,耐高温和良好的低温性能。如果在汽车的一些零件上加一次锂润滑剂,就足以用到汽车报废为止。
在冶金工业上,利用锂能强烈地和氧、氮、氯、硫等物质反应的性质,充当脱氧剂和脱硫剂。在铜的冶炼过程中,加入十万分之一到万分之一的锂,能改善铜的内部结构,使之变得更加致密,从而提高铜的导电性。锂在铸造优质铜铸件中能除去有害的杂质和气体。在现代需要的优质特殊合金钢材中,锂是清除杂质最理想的材料。
1kg锂燃烧后可释放42998kJ的热量,因此锂是用来作为火箭燃料的最佳金属之一。1kg锂通过热核反应放出的能量相当于二万多吨优质煤的燃烧。若用锂或锂的化合物制成固体燃料来代替固体推进剂,用作火箭、导弹、宇宙飞船的推动力,不仅能量高、燃速大,而且有极高的比冲量,火箭的有效载荷直接取决于比冲量的大小。
如果在玻璃制造中加入锂,锂玻璃的溶解性只是普通玻璃的1/100(每一普通玻璃杯热茶中大约有万分之一克玻璃),加入锂后使玻璃成为"永不溶解",并可以抗酸腐蚀。
纯铝太软,当在铝中加入少量的锂、镁、铍等金属熔成合金,既轻便,又特别坚硬,用这种合金来制造飞机,能使飞机减轻2/3的重量,一架锂飞机两个人就可以抬走。锂-铅合金是一种良好的减摩材料。
真正使锂成为举世瞩目的金属,还是在它的优异的核性能被发现之后。由于它在原子能工业上的独特性能,人称它为"高能金属"。
锂电池是二十世纪三、四十年代才研制开发的优质能源,它以开路电压高,比能量高,工作温度范围宽,放电平衡,自放电子等优点,已被广泛应用于各种领域,是很有前途的动力电池。用锂电池发电来开动汽车,行车费只有普通汽油发动机车的1/3。由锂制取氚,用来发动原子电池组,中间不需要充电,可连续工作20年。要解决汽车的用油危机和排气污染,重要途径之一就是发展向锂电池这样的新型电池。
 锂的商业用途
锂的商业用途 锂化合物早先的重要用途之一是用于陶瓷制品中,特别是用于搪瓷制品中,锂化合物的主要作用是作助熔剂。
氟化锂对紫外线有极高的透明度,用它制造的玻璃可以洞察隐蔽在银河系最深处的奥秘。锂玻璃可用来制造电视机显像管。
二战期间,美国飞行员备有轻便应急的氢气源-氢化锂丸。当飞机失事坠落在水面时,只要一碰到水,氢化锂就立即溶解释放出大量的氢气,使救生设备充气膨胀.
用氘化锂和氚化锂来代替氘和氚装在氢弹里充当炸药,达到氢弹爆炸的目的。中国于1967年6月17日成功爆炸的第一颗氢弹里就是利用氘化锂。
 锂的焰色
锂的焰色 硼氢化锂和氢化铝锂,在有机化学反应中被广泛用做还原剂,硼氢化锂能还原醛类、酮类和酯类等。氢化铝锂,是制备药物、香料和精细有机化学药品等中重要的还原剂。氢化铝锂,也可用作喷气燃料。氢化铝锂是对复杂分子的特殊键合的强还原剂,这种试剂已成为许多有机合成的重要试剂。
有机锂化合物与有机酸反应,得到能水解成酮的加成产物,这种反应被用于维生素A合成的一步。有机锂化物加成到醛和酮上,得到水解时能产生醇的加成产物。
由锂和氨反应制得的氨基锂被用来引入氨基,也被用作脱卤试剂和催化剂。
当狼吃下含有锂化合物的肉食后,能引起消化不良,食欲大减,从而改变狼食肉的习性,这种习性还具有遗传性。
人类对金属锂的应用已有了良好的开端,但由于锂的生产工艺比较复杂,成本很高。如果人们一旦解决了这些问题,锂的优良性能将得到进一步的发挥,从而扩大它的应用范围。
锂能改善造血功能,提高人体免疫机能。锂对中枢神经活动有调节作用,能镇静、安神,控制神经紊乱。锂可置换替代钠,防治心血管疾病。人体每日需摄入锂0.1mg左右。
锂的生物必需性及人体健康效应。锂是有效的情绪稳定剂。随着新的情绪稳定剂的出现,对锂治疗的兴趣和研究虽已减少,但锂仍是治疗急性躁狂症和躁狂-抑郁病预防性管理的最有效措施。许多研究证明,锂对动物和人具有必需功能或有益作用。动物缺锂可导致寿命缩短、生殖异常、行为改变及其他异常。人类流行病学研究显示,饮水锂浓度与精神病住院率、杀人、自杀、抢劫、暴力犯罪和毒品犯罪率呈显著负相关。毒品犯的营养性锂补充研究证明锂有改善和稳定情绪的作用。心脏病人、学习低能者和在押暴力犯发锂含量显著降低。碳酸锂治疗的临床研究表明,锂的主要反应器官为胃肠道、肾脏、神经、肌肉、内分泌和心血管系统。在170~228mgLi/d治疗剂量范围内,预期的血清锂水平为0.4~0.8 mEq/L(2.78~5.55 mg/L),无毒性反应。在锂的危险性评估中,对治疗剂量采用10倍安全因子对孕妇和胎儿不造成危害,这相当于成人每天摄入2mg Li。动物的NOAEL(无毒性作用水平)为10 mgLi/kg/d,采用32倍安全因子,得到日允许摄入量(ADI)为0.31mgLi/kg/d。基于动物实验数据,锂的表观缺乏摄入量为:山羊:<1.5mgLi/kg,大鼠:<15 μgLi/kg。人对锂的饮食需要量约为60~100 μg/d,典型的日摄入量为200~600μg。蛋类、牛奶、奶制品、鱼类、土豆和蔬菜含有丰富的锂。
与钾、钠类似,金属锂很活泼,需隔绝空气储存。
贮存和使用都要注意安全,由金属锂引起的火灾,不能用水或泡沫灭火剂扑灭,而要用碳酸钠干粉。锂也对皮肤有很强的腐蚀性。